探索手性分子基础:走进手性分子的奇妙世界
手性:一个物体若与其镜像不能重合,称这个物体具有手性;也叫手征性。
不能与自身镜像重合的分子称为手性分子。一个分子是否具有手性与其对称性有关:
对称面:
若有一个平面把分子分成两半,这两半是实物与镜像的关系,则此平面是分子的对称面。用σ表示。

对称中心:
若分子中有一点,从分子中的任一原子或基团出发,向该点引一直线,若在距该点等距离处,有一相同的原子或基团,这点是对称中心,用i表示。

凡是分子中具有对称面或对称中心的分子是非手性分子;反之分子具有手性。
凡是手性分子必有互为镜像的两种构型,互为镜像的两种构型的异构体叫做一对对映体。这种立体异构称为对映异构。
注意:要把一种构型转变成它的对映异构体,必须断裂分子中的化学键,然后对调两个基团的位置。
手性碳原子:连有四个不同基团的碳原子。
注:
1.若分子中仅有一个手性碳原子,则该分子为手性分子,就存在一对对映异构体。
2.有些分子不含手性碳原子,但其仍为手性分子。
3.有的分子中含有多个手性碳原子,但其不是手性分子。(如下图)
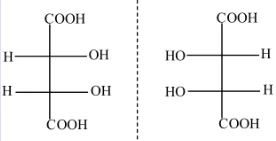
内消旋体:
内消旋体是指分子内具有2个或多个非对称中心,但又有其他对称因素,如对称面存在,因而使整个分子不具有旋光性的化合物。
外消旋体:
外消旋体是一种具有旋光性(见旋光异构)的手性分子(见手征性)与其对映体的等摩尔混合物。
内消旋体与外消旋体的异同:
1)二者都无旋光性;
2)内消旋体是纯的非手性物质,而外消旋体是对对映体的等量混合物;
3)内消旋体不可拆分,而外消旋体可拆分。
一对对映体,它们的一般物理性质(如:熔沸点、密度、折光率、在非手溶剂中的溶解度以及光谱性质)相同但它们对偏振光的作用不同。
1、偏振光:
偏振光是指光波的电场在传播方向上的振动被限制在一个平面内,且该平面与光的传播方向垂直。这种现象使得光波在垂直于传播方向的截面上,其电场端点的轨迹形成一条直线、一个圆或一个椭圆。
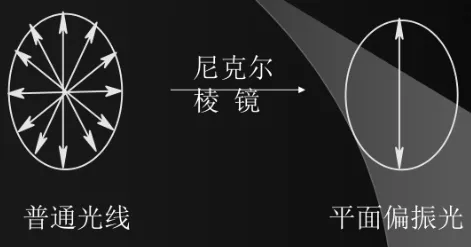
2、旋光性:
能使偏振光发生偏转的性质,称为旋光性;具有这种性质的物质,称为旋光性物质(光活性物质);反之为非光活性物质。使偏振光振动方向旋转的角度称为旋光度,用α表示。使偏振光振动方向向左旋称为左旋体,用“一”表示;向右旋的称为右旋体,用“+”表示。

注:
①凡是手性分子,都有旋光性;非手性分子无旋光性。
②一对对映体对偏振光的作用正好相反,一个使偏振光左旋,一个使之右旋,旋光度数值相等。
3、旋光性的测量:
用旋光仪进行测量
旋光仪主要由一个光源、两个尼克尔棱镜和一个盛测试样品的盛液管组成。尼克尔棱镜是由两块方解石直角棱镜沿斜面用加拿大树脂粘合而成。当一束单色光照射到尼克尔棱镜时,分解为两束相互垂直的平面偏振光,一束折射率为1.658的寻常光,一束折射率为1.486的非寻常光,这两束光线到达加拿大树脂粘合面时,折射率大的寻常光被全反射到底面上的墨色涂层被吸收,而折射率小的非寻常光则通过棱镜,这样就获得了一束单一的平面偏振光。

4、比旋光度的计算:

物理意义:1mL含1g旋光性物质的溶液,在1dm长的盛样管中,利用一定波长的入射光(钠单色光,D,λ=586.3nm)测得的旋光度。
比旋光度与入射光的波长、温度和溶剂有关,常将[α]写作[α]λt葡萄糖:[α]D25 =+ 52.5。
在不用水做溶剂时,需注明溶剂的名称:
(5%乙醇)酒石酸在5%的乙醇溶液中其比旋光度为[α]D25=+ 3.79°(5%乙醇)。
1、手性碳:常用“*”表示

含有一个手性碳原子的化合物,一定是手性分子。有一对对映体,其中一个是左旋,一个是右旋。如乳酸:
[α]D15 =+ 3.8。 [α]D15=-3.8。
外消旋体:等量的左、右旋体的混合物
注意:
①外消旋体没有旋光性;
②外消旋体与其左、右旋体的物理性质不同;
③一般的物理方法不能分离外消旋体。
2、构型的表示方法
1)球棒模型

2)透视型(或伞形式)
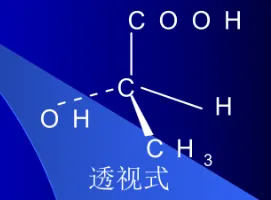
“楔前虚后实平面”
3)菲舍尔(Fischer)投影式
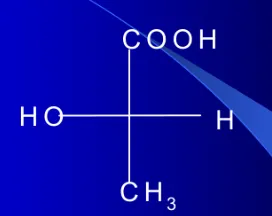
投影规则:
①手性碳放在纸面上,
②伸向纸面前方的键放在横键上,伸向纸面后方的键放在竖键上(横前竖后);
③主链竖着写,命名时编号小的碳在最上方。
3、构型的标记
1)D-L标记法--相对构型标记
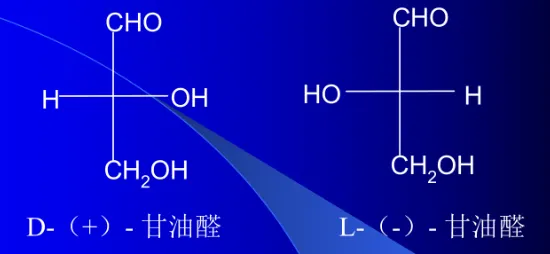
注:D、L与左右旋无关,D、L表示相对构型而左、右旋通过旋光仪测定结果。
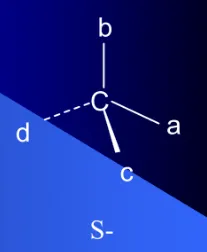
2)R-S标记法--绝对构型标记法取代基的优先次序规则:
取代基按其第一个原子的原子序数大小排列,原子序数大者为“较优”基团。若为同位素,则质量重的定为“较优”基团.
I>Br>CI>F>OH>NH2>CH3>D>H
②如果两个基团的第一个原子相同,则比较与之相连的第二个原子,以此类推。
-CH2CH3 >CH3

③含有双键或叁键基团,可以分解为连有两个或三个相同原子。

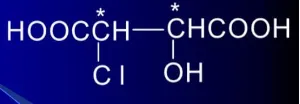
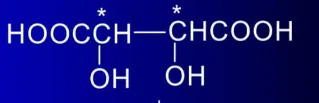
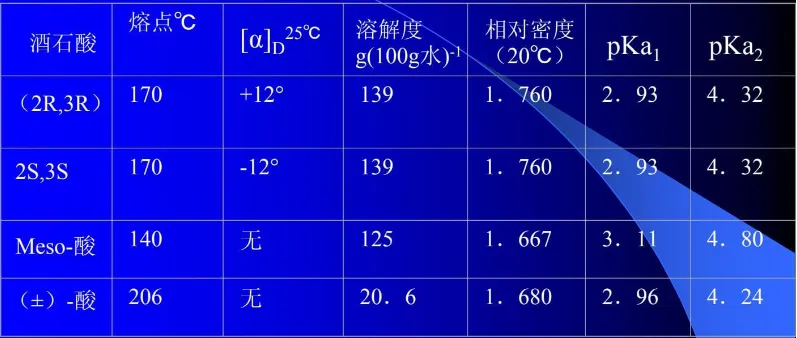
标记方法: 若a>b>c>d,d在离视线最远处; 若a>b>c为“顺”—R型 若a>b>c为“逆”—S型 含有两个不同手性碳原子的化合物 2-羟基-3-氯丁二酸(氯代苹果酸) 表:氯代苹果酸的物理性质 含有两个相同手性碳原子的化合物 2,3-二羟基丁二酸(酒石酸)是内消旋体 表:酒石酸的物理性质 总之,手性分子是一个充满奇妙和未知的世界。它们不仅构成了生命的基础,还推动了化学、生物学和药学等领域的发展。未来,随着科技的进步和研究的深入,我们相信会有更多关于手性分子的奇妙发现等待我们去探索。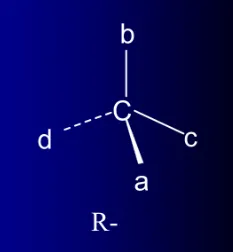



 地址:广州市黄埔区揽月路3号国际企业孵化器F座310
地址:广州市黄埔区揽月路3号国际企业孵化器F座310 电话:18922204815
电话:18922204815  传真:020-84418344
传真:020-84418344 邮箱:mzzhang@chiral-se.com
邮箱:mzzhang@chiral-se.com

